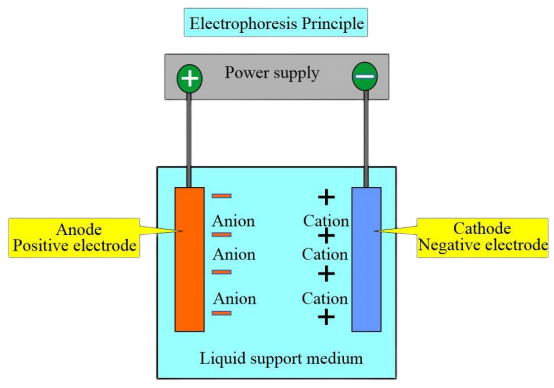
Principi de l'experimentació
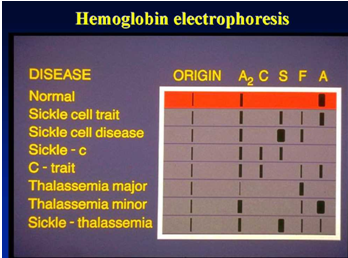
L'electroforesi de l'hemoglobina té com a objectiu detectar i confirmar diverses hemoglobines normals i anormals.
A causa de les diferents càrregues i punts isoelèctrics dels diferents tipus d'hemoglobina, en una determinada solució tampó de pH, quan el punt isoelèctric de l'hemoglobina és inferior al pH de la solució tampó, l'hemoglobina porta una càrrega negativa i migra cap a l'ànode durant l'electroforesi. Per contra, l'hemoglobina amb càrrega positiva es mou cap al càtode.
Sota un determinat voltatge i després d'un temps d'electroforesi específic, les hemoglobines amb diferents càrregues i pesos moleculars presenten diferents direccions i velocitats de migració. Això permet la separació de zones diferents i es poden realitzar posteriors anàlisis d'exploració colorimètrica o electroforètica en aquestes zones per quantificar diverses hemoglobines. El mètode més utilitzat és l'electroforesi de membrana d'acetat de cel·lulosa de pH 8,6.
Dins del citoplasma, els grups etilenglicol (CHOH-CHOH) presents en substàncies de glicogen o polisacàrids (com ara mucopolisacàrids, mucoproteïnes, glicoproteïnes, glicolípids, etc.) s'oxiden per l'àcid periòdic i es converteixen en grups aldehids (CHO-CHO). Aquests grups aldehids es combinen amb el reactiu incolor de Schiff vermell porpra, formant un colorant vermell morat que es diposita on hi ha polisacàrids a la cèl·lula. Aquesta reacció es coneix com a tinció periòdica d'àcid-Schiff (PAS), abans anomenada tinció de glicogen.
Mètode d'experimentació
Materials:Acetat de cel·lulosamembrana, aparell d'electroforesi(DYCP-38C i font d'alimentació DYY-6C), Eina de càrrega de mostres superior (pipeta), espectrofotòmetre, cubetes colorimètriques, amortidors.
Buffer:
(1) Tampó pH 8,6 TEB: peseu 10,29 g de Tris, 0,6 g d'EDTA, 3,2 g d'àcid bòric i afegiu aigua destil·lada a 1000 ml.
(2) Tampó borat: peseu 6,87 g de bòrax i 5,56 g d'àcid bòric i afegiu aigua destil·lada a 1000 ml.
Procediment:
Preparació de la solució d'hemoglobina
Prendre 3 ml de sang que contingui heparina o citrat de sodi com a anticoagulant. Centrifugar a 2000 rpm durant 10 minuts i descartar el plasma. Rentar els glòbuls vermells tres vegades amb solució salina fisiològica (750 rpm, 5 minuts de centrifugació cada vegada). Centrifugar a 2200 rpm durant 10 minuts i descartar el sobrenedant. Afegiu una quantitat igual d'aigua destil·lada, després afegiu 0,5 vegades el volum de tetraclorur de carboni. Agiteu enèrgicament durant 5 minuts, i després centrifugueu a 2200 rpm durant 10 minuts per recollir la solució de Hb superior per utilitzar-la posteriorment.
Remull de la membrana
Talleu la membrana d'acetat de cel·lulosa en tires de 3 cm × 8 cm. Remullar-los en tampó de pH 8,6 TEB fins que estiguin completament saturats, després treure i assecar amb paper de filtre.
Localització
Utilitzeu una pipeta per detectar 10 μl de la solució d'hemoglobina verticalment a la membrana d'acetat de cel·lulosa (la part rugosa), a uns 1,5 cm de la vora.
Electroforesi
Aboqueu la solució tampó de borat a la cambra d'electroforesi. Col·loqueu la membrana d'acetat de cel·lulosa amb el costat tacat a l'extrem del càtode de la cambra. Funciona a 200 V durant 30 minuts.
Elució
Retalleu les zones HbA i HbA2, col·loqueu-les en tubs d'assaig separats i afegiu 15 ml i 3 ml d'aigua destil·lada, respectivament. Agiteu suaument per diluir l'hemoglobina completament i després barregeu-lo.
Colorimetria
Posar a zero l'absorbància utilitzant aigua destil·lada per a la solució d'elució i mesurar l'absorbància a 415 nm.
Càlcul
HbA2(%) = Absorbància del tub HbA2 / (Absorbància del tub HbA × 5 + Absorbància del tub HbA2) × 100%
Càlcul de resultats experimentals
Interval de referència per a pH 8,6 TEB Tampó acetat de cel·lulosa Electroforesi: HbA > 95%, HbA2 1%-3,1%
Notes
El temps d'electroforesi no hauria de ser massa llarg. La membrana d'acetat de cel·lulosa no s'ha d'assecar durant l'electroforesi. Atureu l'electroforesi quan HbA i HbA2 estiguin clarament separats. L'electroforesi prolongada pot provocar difusió i desenfocament de la banda.
Eviteu utilitzar massa mostra. L'excés de líquid d'hemoglobina pot provocar un despreniment de la banda o una tinció insuficient, donant lloc a nivells d'HbA falsament elevats.
Evitar la contaminació de la membrana d'acetat de cel·lulosa amb proteïnes.
El corrent no ha de ser massa alt; en cas contrari, les bandes d'hemoglobina poden no separar-se.
Incloeu sempre mostres d'individus normals i hemoglobines anormals necessàries com a controls.
Beijing Liuyi Biotechnology fabrica el tanc d'electroforesi professional per a electroforesi d'hemoglobina que és el modelDYCP-38CTanc d'electroforesi de membrana d'acetat de cel·lulosa i hi ha dos models d'alimentació d'electroforesi disponibles per al tanc d'electroforesi de membrana d'acetat de cel·lulosaDYY-2CiDYY-6Cfont d'alimentació.
Mentrestant, Beijing Liuyi Biotechnology proporciona membrana d'acetat de cel·lulosa per als clients i la mida de la membrana d'acetat de cel·lulosa es pot personalitzar. Benvingut a demanar-nos mostres i més informació.
La marca Beijing Liuyi té més de 50 anys d'història a la Xina i l'empresa pot oferir productes estables i d'alta qualitat a tot el món. A través d'anys de desenvolupament, és digne de la vostra elecció!
Ara estem buscant socis, tant el tanc d'electroforesi OEM com els distribuïdors són benvinguts.
Si teniu algun pla de compra dels nostres productes, no dubteu a posar-vos en contacte amb nosaltres. Podeu enviar-nos un missatge al correu electrònic[correu electrònic protegit]o[correu electrònic protegit], o truca'ns al +86 15810650221 o afegeix Whatsapp +86 15810650221 o Wechat: 15810650221
Hora de publicació: 20-set-2023